Co sprawia, że niektórzy ciężko przechodzą zarażenie COVID-19?
Zespół kanadyjskich naukowców z Lawson Health Research Institute i Western University opublikował wyniki dwóch badań, które mogą pomóc w radzeniu sobie z koronawirusem. W jednym badacze odkryli, że we krwi chorych na COVID-19 są substancje, które zwiastują ciężki przebieg choroby, a w drugim wykazali, jak dochodzi do zagrażających życiu skrzepów.
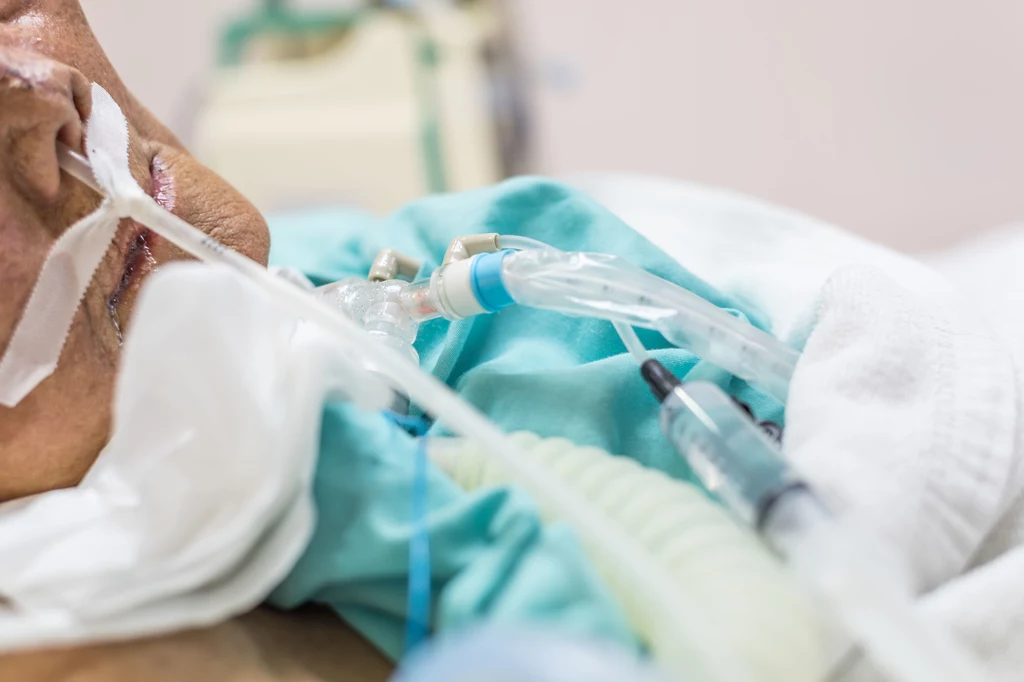
Część osób zakażonych koronawirusem przechodzi chorobę łagodnie, a nawet bezobjawowo, ale niektórzy zapadają na ciężką postać COVID-19.
Dotąd nie można było z wyprzedzeniem określić, kogo to będzie dotyczyło. Zagadką było też to, jak dochodzi do jednego z głównych powikłań u krytycznie chorych pacjentów. Chodzi o pojawiające się w płucach skrzepy, które utrudniają natlenienie organizmu.
Na łamach pisma "Critical Care Explorations" zespół złożony z naukowców z Lawson Health Research Institute i Western University wskazał drogę do rozwiązania tych problemów.
- Zaczęliśmy dostarczać odpowiedzi na jedne z najważniejszych pytań odnośnie COVID-19 zadawanych przez klinicystów i zajmujących się zdrowiem naukowców - podkreśla kierujący pracami dr Douglas Fraser.
- Wyniki muszą zostać jeszcze potwierdzone w badaniach na większej grupie pacjentów, ale mogą mieć ważne konsekwencje dla leczenia i badania choroby - dodaje.
Naukowcy zwracają uwagę, że przy braku odpowiednich metod leczenia, wielu chorych z COVID-19 przyjmowanych na oddziały intensywnej terapii nie przeżywa.
Lipa – naturalny lek na przeziębienie
Lipa to naturalne remedium na wiele dolegliwości. Pomoże przy dyskomforcie trawiennym, przeziębieniu, a także zszarganych nerwach. Początek lipca to najlepszy czas, by zainteresować się zbiorem pięknie pachnących kwiatów lipy.






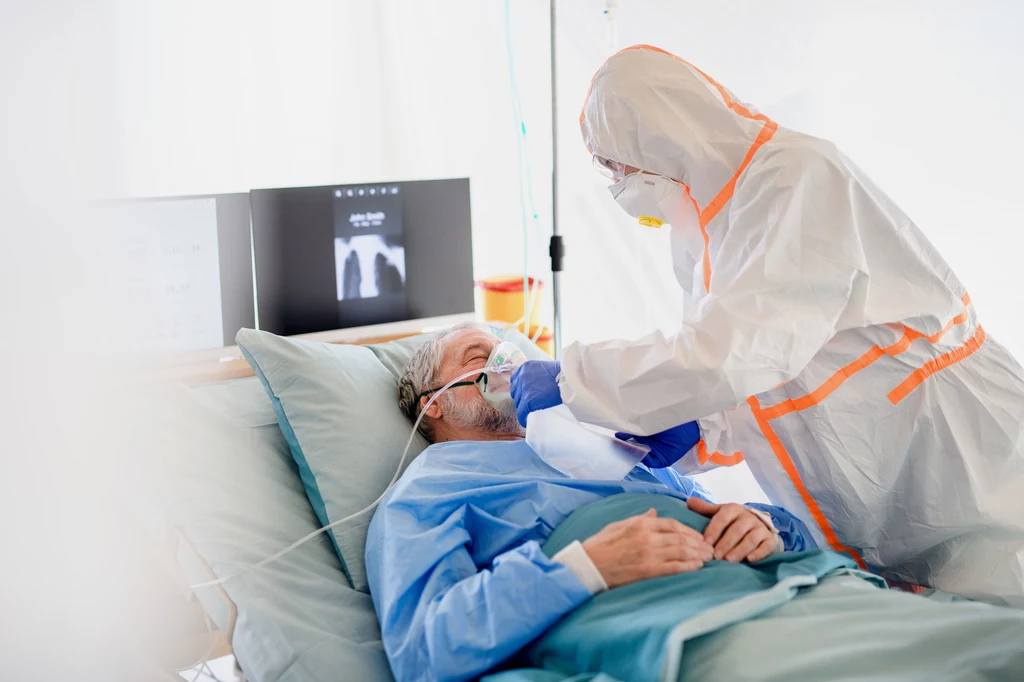
- Kiedy pacjent zostaje przyjęty na oddział intensywnej terapii, zwykle czekamy, aby zobaczyć, czy mu się pogorszy, zanim rozpatrzymy jakieś ryzykowne interwencje. Aby poprawić szanse chorego, potrzebujemy nie tylko nowych terapii, ale także sposobów przewidywania, który pacjent będzie w złym stanie - tłumaczy dr Fraser.
W jednym z dwóch badań, polegającym na analizie krwi 30 chorych, naukowcy zidentyfikowali cząsteczki sześciu substancji, które w podwyższonym stężeniu wskazują na przyszły ciężki przebieg choroby.
Określenie poziomu tych substancji może więc pomóc w dobraniu najlepszego leczenia i zdobyciu na czas odpowiednich do tego środków. Lekarze będą też mogli odpowiednio przygotować rodzinę oraz samych pacjentów.
Wiedza na temat tych cząsteczek pomoże też w prowadzeniu lepszej jakości badań klinicznych, ponieważ będzie można w nich grupować ochotników według ich indywidualnego ryzyka.
W drugim badaniu natomiast naukowcy z Kanady odkryli, skąd u ciężko chorych biorą się groźne skrzepy w płucach.
- Powód powstawania skrzepów był niejasny. Większość ekspertów podejrzewała, że normalny system krzepliwości był zbyt mocno pobudzany, więc wielu lekarzy próbowało stosować środki przeciwzakrzepowe, takie jak heparyna. Jednak odkryliśmy zupełnie inny mechanizm - mówi dr Fraser.
Analiza krwi pacjentów pokazała, że u chorych na COVID-19 warstwa wyściełająca naczynia krwionośne ulega uszkodzeniu i powstają w niej stany zapalne. W ten sposób powstaje środowisko, które sprzyja przyłączaniu się powodujących krzepnięcie płytek krwi.
Badacze odkryli, że pacjenci z COVID-19 mają większe stężenie trzech substancji. Dwie z nich powstają z rozpadu małych, przypominających włoski struktur (glikokaliksu), które znajdują się na ściankach naczyń. Natomiast jedna pomaga płytkom łączyć się z naczyniami.
- Glikokaliks zapobiega przyłączaniu się płytek do wnętrza naczyń i wspomaga produkcję tlenku azotu, który odgrywa ważną rolę w zapobieganiu przyłączania się płytek - wyjaśnia dr Fraser.
- Podejrzewamy, że odpowiedź immunologiczna powoduje powstanie enzymów uszkadzających te podobne do włosków struktury, wywołuje zapalenie naczyń, które zaczynają przyciągać powodujące skrzepy płytki - kontynuuje specjalista.
Zdaniem badaczy mogłyby pomóc dwie terapie. Jedna to wykorzystanie inhibitorów płytek zapobiegających przyłączaniu się ich do ścianek naczyń. Druga polegałaby na użyciu cząsteczek chroniących naczynia i przywracających naturalną budowę ich ścianek.
- Sprawdzenie tych terapii jako potencjalnej alternatywy dla środków przeciwzakrzepowych może poprawić szanse pacjentów. Dzięki obu naszym odkryciom mamy nadzieję na opracowanie narzędzi do prognozowania, którzy pacjenci będą najbardziej chorzy oraz metod leczenia zapaleń oraz skrzepów - mówi dr Fraser.
***
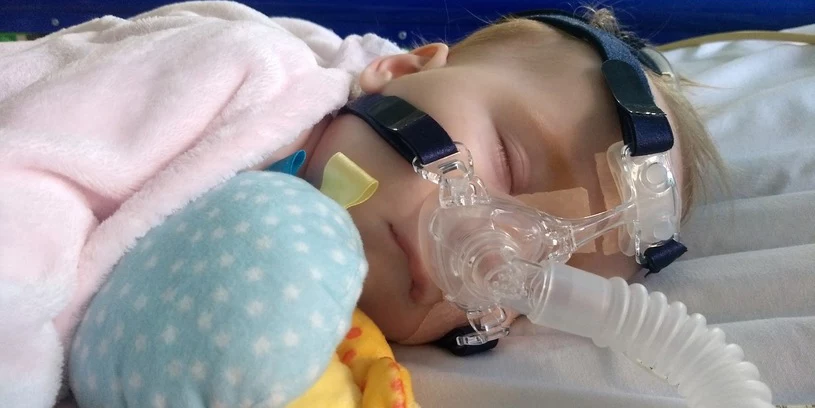
Hania ma 17 miesięcy i SMA1 - rdzeniowy zanik mięśni. Innowacyjna terapia genowa kosztuje ponad 9 milionów złotych. Środki potrzebne są jak najszybciej, bo warunkiem przystąpienia do leczenia jest rozpoczęcie go przed ukończeniem drugiego roku życia. Niestety, w prowadzonej od sześciu miesięcy zbiórce, nadal brakuje ponad czterech milionów złotych.
JEŚLI MOŻESZ, WESPRZYJ ZBIÓRKĘ: www.siepomaga.pl/haneczka
Przeczytaj historię Hani: Bez terapii genowej Hania nie ma szans. Pomóż dokończyć zbiórkę









